一、研究目标
该研究旨在开发一种适用于吞咽障碍人群的功能性食品,同时实现脂溶性营养素(β-胡萝卜素)的高效包载与控释。具体目标包括:
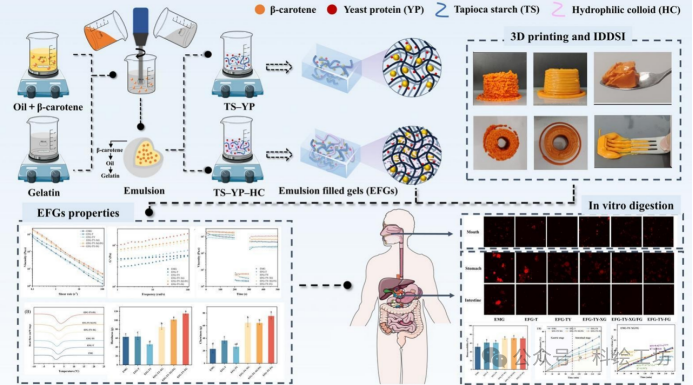
1. 构建以木薯淀粉、酵母蛋白和亲水胶体为连续相的乳液填充凝胶;
2. 评估其3D打印性能、流变学特性、热稳定性及微观结构;
3. 研究其在体外模拟消化过程中对β-胡萝卜素的保护与释放行为;
4. 验证其是否符合国际吞咽障碍饮食标准化倡议(IDDSI)5级标准。
二、创新点
1. 构建三元复合凝胶基质(TS-YP-HC)用于β-胡萝卜素递送将木薯淀粉、酵母蛋白与亲水胶体(黄原胶、亚麻籽胶等)复合,形成致密的三维网络结构,显著提升了凝胶的力学性能与结构稳定性。
2. 系统揭示亲水胶体在调控凝胶结构与功能中的作用机制通过流变学、热分析、微观结构观察等手段,阐明了亲水胶体如何通过增强分子间相互作用(如氢键、疏水作用)来提升凝胶的网络致密性、油滴固定能力和热稳定性。
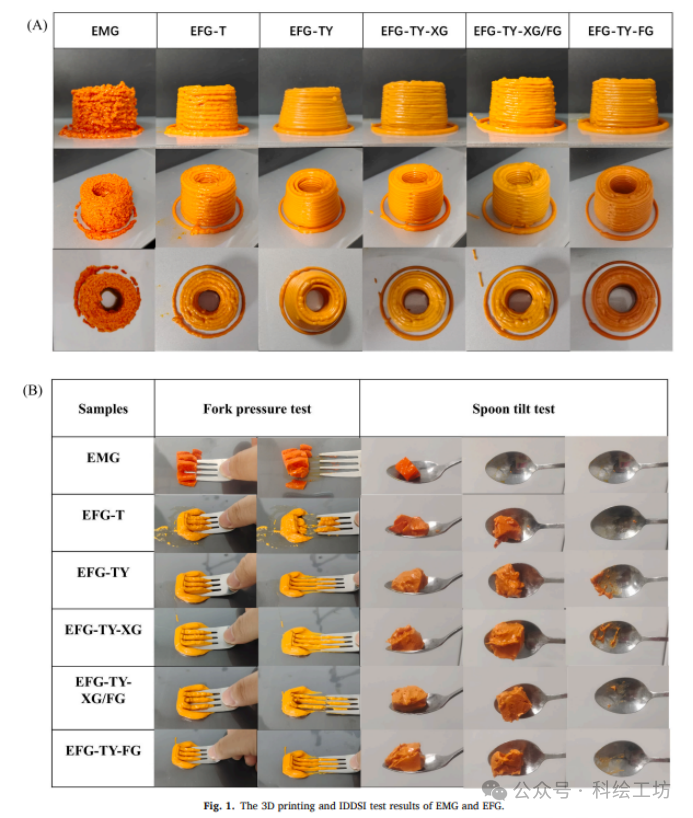
3. 结合3D打印与IDDSI标准,实现吞咽友好食品的精准构建将3D打印技术引入吞咽障碍食品开发中,通过调控凝胶的流变特性与机械强度,实现了结构可控、营养强化、吞咽安全的功能性食品设计。
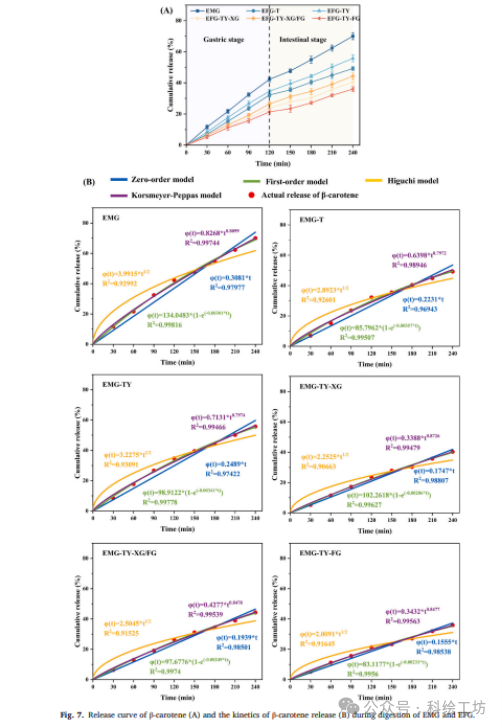
4. 深入解析β-胡萝卜素的释放动力学机制采用Korsmeyer-Peppas等释放动力学模型,揭示了β-胡萝卜素在消化过程中的非Fickian扩散机制,即扩散与基质溶胀/侵蚀协同调控释放行为。
三、主要实验与理论方法
1. 样品制备β-胡萝卜素乳液:以玉米油为油相,明胶为乳化剂,制备O/W乳液;凝胶基质构建:分别以TS、TS-YP、TS-YP-HC为连续相,与乳液混合后冷却形成乳液填充凝胶;3D打印:使用食品级3D打印机,设定标准参数打印中空圆柱模型。
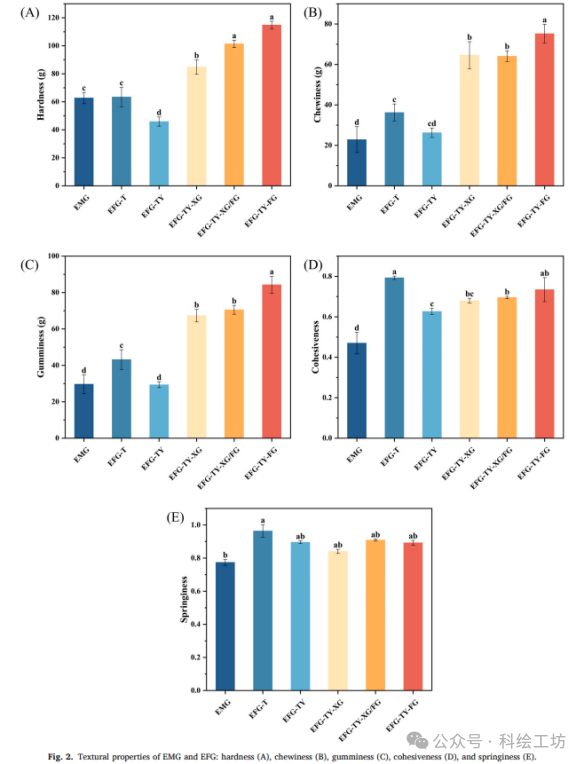
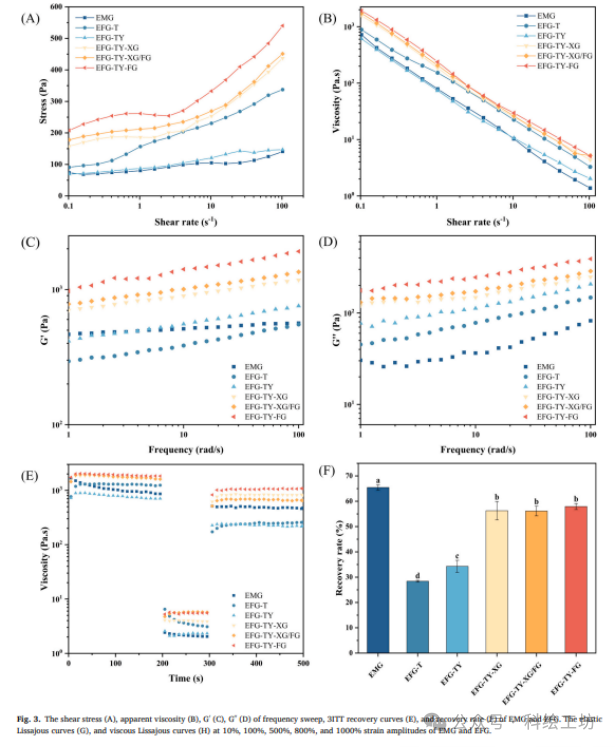
2. 性能表征流变学测试:包括稳态剪切、频率扫描、三阶段触变性测试、大振幅振荡剪切(LAOS)分析;质构分析:测定硬度、咀嚼性、胶粘性、弹性等;热分析:差示扫描量热法(DSC)测定冰晶形成与熔融温度;微观结构:共聚焦激光扫描显微镜(CLSM)观察消化过程中油滴分布;β-胡萝卜素含量测定:紫外-可见分光光度法。
3. 体外消化与释放动力学模拟口腔-胃-小肠三阶段消化;测定β-胡萝卜素的释放曲线,并拟合零级、一级、Higuchi、Korsmeyer-Peppas模型;计算生物可及性。
四、机制阐释
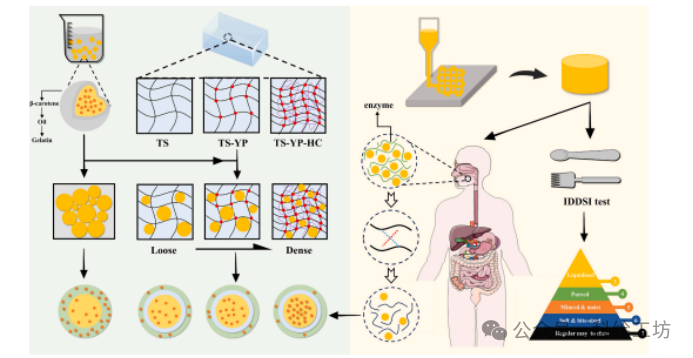
该研究的创新之处不在于首次使用淀粉或蛋白,而在于深刻揭示了亲水胶体如何通过“分子桥梁”作用,对整个体系的微观结构进行重编程,从而调控宏观性能。
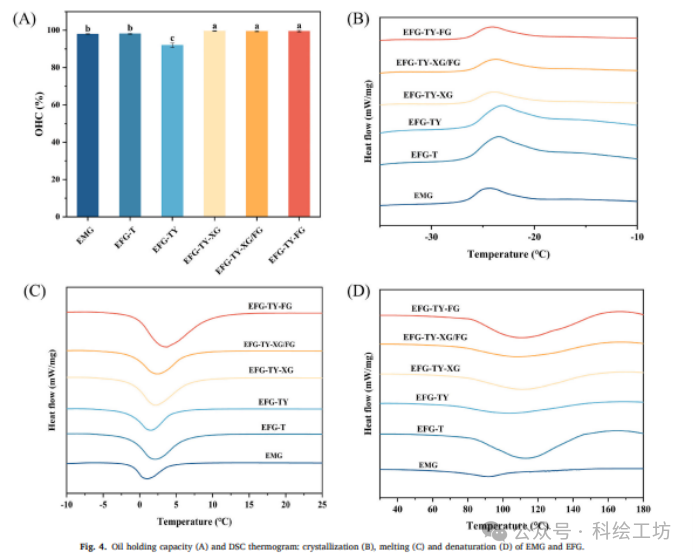
机理一:亲水胶体作为“网络增强剂”,构建致密的双连续相屏障从宏观现象切入:实验观察到,添加亲水胶体(HC)的EFG-TY-HC体系,其硬度和持油性远高于无胶体的EFG-TY,甚至优于纯淀粉体系。深入分子层面解读:为什么?单纯的淀粉-酵母蛋白(TS-YP)网络是“脆弱”的。酵母蛋白的加入,虽然增加了营养,但其分子可能干扰了淀粉分子间的氢键重排,导致网络结构松散(EFG-TY的Tc升高、硬度下降的直接证据)。而当亲水胶体(XG/FG)加入后,情况发生了质变。这些线性多糖长链,凭借其强大的亲水性和分子缠结能力,同时与溶出的直链淀粉和蛋白质分子发生相互作用,形成了一个贯穿整个体系的“二级网络”。这个网络不仅填充了淀粉-蛋白网络的空隙,还像“钢筋”一样加固了整个凝胶结构。结果:这种双网络结构实现了两大功能:一是物理性地“锁住”了乳液油滴,解释了OHC的提升;二是限制了水分子的运动,导致可冻结水含量降低,Tc向低温移动,从而提升了冻融和热稳定性。
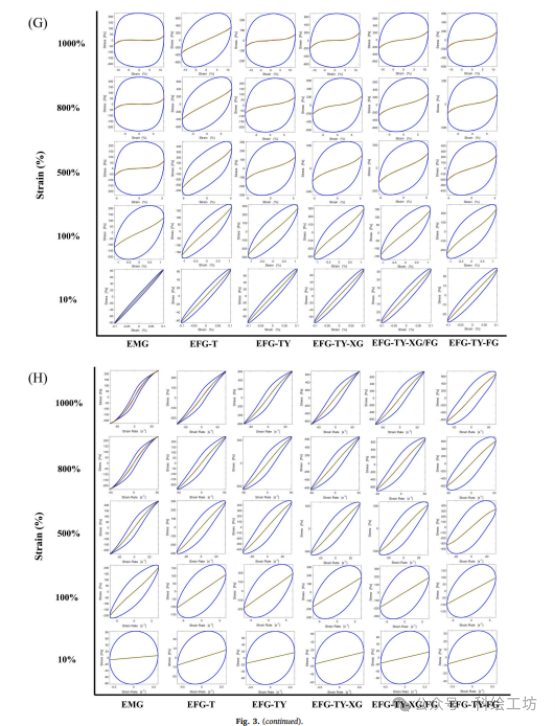
机理二:通过“流变学编程”实现吞咽安全与3D打印精度的统一从应用场景出发:吞咽友好食品要求低应力下易流动(口腔处理),但沉积后能迅速恢复强度(保持形状)。3D打印则要求墨水既能顺畅挤出,又能层层堆叠不坍塌。解读流变学证据:研究通过SAOS和LAOS测试,揭示了其中的精妙平衡。线性区(SAOS):EFG-TY-HC的G'最高,表明其静态结构最强,这是打印后形状保真的基础。非线性区(LAOS):随着应变增加,所有样品都出现剪切变稀。但EFG-TY-HC的Lissajous曲线在低应变下面积更大(能量耗散更强),表明其在受力时能更有效地耗散能量,防止结构突然脆性断裂,这对于避免在吞咽过程中形成危险的大碎片至关重要。触变性(3-ITT):HC的加入使得体系在经历高剪切后能快速恢复(RR高达80%以上)。这意味着在3D打印时,墨水通过喷嘴的瞬间粘度降低(顺利挤出),一旦沉积下来,粘度迅速回升(支撑上层),完美诠释了“剪切变稀-快速回复”的理想流变行为。
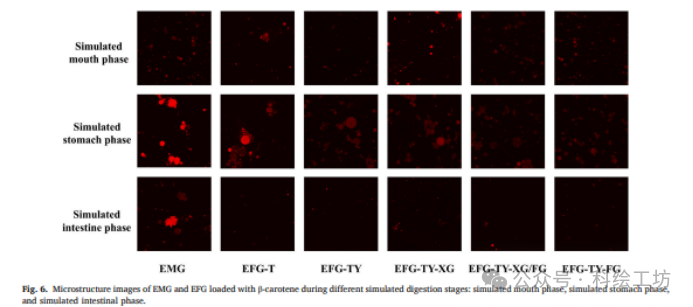
机理三:从“被动包埋”到“智能控释”——非Fickian扩散的生物学意义关键发现:体外消化实验显示,EFG-TY-HC不仅保护了β-胡萝卜素在胃中不被过早释放(释放率最低),还在肠道中实现了持续释放。动力学模型解读:Korsmeyer-Peppas模型拟合得到的n值(0.80-0.87)极具深意。它明确告诉我们,释放机制不是简单的Fickian扩散(浓度梯度驱动),而是扩散与骨架溶蚀的协同作用(非Fickian扩散)。生物学意义:这种机制是“智能”的。在胃的酸性环境和高离子强度下,凝胶网络收缩,主要靠扩散(极慢);进入肠道后,胰酶开始水解淀粉和蛋白网络,骨架开始“溶蚀”,被紧密包裹的油滴暴露出来,从而触发释放。这与CLSM图像中观察到的肠道阶段油滴释放和尺寸减小的现象完全吻合。HC的存在,通过增强网络致密性,减缓了溶蚀速度,从而实现了“缓释”。
五、结论展望
该研究通过系统构建与表征TS-YP-HC三元复合凝胶体系,不仅实现了β-胡萝卜素的高效包载与控释,还成功将其应用于3D打印吞咽友好食品的开发中。研究在材料设计、结构调控、功能评价等方面均具有显著创新性,为功能性凝胶载体的理性设计与个性化营养食品的开发提供了坚实的理论基础与实验依据,具有重要的学术价值与应用前景。
声明
本文是对已发表研究的原创性编译与解读。尊重原作版权,所有权利归原出版方与作者所有。如涉及侵权,请即联系删除。鉴于编译水平,内容或有疏漏,敬请指正。
参考文献 https://doi.org/10.1016/j.foodchem.2026.148555
来源:公众号-科绘工坊
原文链接:https://mp.weixin.qq.com/s/xnXA4hX8HUj9___wODQ_5Q



